EBMT Nursing Education : Cellule souche hématopoïétique Mobilisation et cytaphérèse : Guide pratique à l'usage des infirmiers et autres ...
←
→
Transcription du contenu de la page
Si votre navigateur ne rend pas la page correctement, lisez s'il vous plaît le contenu de la page ci-dessous
EBMT Nursing Education :
Cellule souche hématopoïétique
Mobilisation et cytaphérèse :
Guide pratique à l’usage
des infirmiers et autres
professionnels paramédicaux
12 Novembre 2009
IL’EBMT (European Group for Blood and Marrow Transplantation)
remercie les personnes suivantes pour leur analyse critique
et leur contribution à l’élaboration de ce guide :
Erik Aerts (infirmier diplômé) Suisse
Aleksandra Babic (infirmière diplômée) Italie
Hollie Devine (infirmière diplômée) États-Unis
Françoise Kerache (infirmière diplômée) Allemagne
Arno Mank (infirmier diplômé) Pays-Bas
Harry Schouten (M.D.) Pays-Bas
Nina Worel (M.D.) AutricheCellule souche hématopoïétique
Mobilisation et cytaphérèse :
Guide pratique à l’usage des infirmiers et
autres professionnels paramédicaux
Table des matières
Chapitre 1 : Synthèse sur l’autogreffe de cellules souches hématopoïétiques . . . . . . . . . . . . . . . 1
Chapitre 2 : Mobilisation. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 5
Chapitre 3 : Collecte de cellules souches (cytaphérèse), conservation et ré-injection . . . . . . . . 13
Chapitre 4 : Comment évoquer certains sujets avec les patients. . . . . . . . . . . . . . . . . . . . . . . . . 19
Glossaire. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 23
Bibliographie. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 24
Autres ressources. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 27
Notes. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 28
Table of ContentsChapitre 1 : Synthèse
Chapitre 1 :
Synthèse sur l’autogreffe de cellules souches hématopoïétiques
Les stratégies de traitement du cancer les plus reconnues comprennent la chimiothérapie et la radiothérapie.
L’objectif en administrant une chimiothérapie haute dose et/ou une radiothérapie aux patients présentant des
tumeurs non réfractaires est de réduire la taille tumorale. L’administration de ces traitements dans le respect
des doses élevées et du calendrier intensif qu’ils nécessitent, est souvent limitée par des toxicités d’organes
(par ex. moelle osseuse, cœur et poumon) et par une pancytopénie. Afin de surmonter ces limites liées à
la dose administrée, l’autogreffe de cellules souches hématopoïétiques (ACSH), traitement à haute
dose basé sur l’injection de cellules souches hématopoïétiques, a évolué en un protocole médical permettant
l’administration de doses élevées de médicaments tout en conservant une toxicité acceptable vis-à-vis des
organes et du système hématopoïétique. L’injection de cellules souches autologues après un traitement
intensif permet de « récupérer » la moelle osseuse en rétablissant une hématopoïèse normale. Suite à la
récupération d’un fonctionnement normal de leur moelle osseuse, les patients peuvent être guéris ou recevoir un
traitement anti-cancéreux supplémentaire.1,2
L’autogreffe de cellules souches hématopoïétiques est un protocole médical complexe utilisé pour traiter et
guérir les patients souffrant de diverses maladies malignes et non malignes. Bien que la première information
sur l’utilisation d’une autogreffe dans le traitement du cancer ait été rapportée dans les années 1890,3 la
guérison de patients souffrant de pathologies cancéreuses ne fut documentée qu’en 1978, suite à un essai
clinique mené au National Cancer Institute (Etats-Unis).4 A la suite de ce rapport, des progrès considérables ont
été réalisés dans la pratique de l’autogreffe et des milliers de patients à travers le monde ont bénéficié d’un
traitement réussi de leur maladie grâce à l’utilisation de l’autogreffe.
Le terme « autogreffe de cellules souches hématopoïétiques » est souvent employé comme synonyme des termes
autogreffe de la moelle osseuse, autogreffe des cellules souches du sang périphérique et autogreffe de cellules
hématopoïétiques.5 « Autogreffe » signifie que les cellules du donneur utilisées dans le protocole proviennent
du patient lui-même, par opposition à « allogénique » où elles proviennent de cellules d’un donneur différent
du patient. Dans certains cas de greffe allogénique, le terme « syngénique » est utilisé lorsque le donneur de
cellules est un jumeau monozygote du patient. La source de la collecte des cellules souches est identifiée par les
termes « moelle osseuse » et « sang périphérique ». Les cellules nécessaires au patient peuvent être prélevées
soit directement dans la moelle osseuse du donneur, telles que celles de la crête iliaque des os pelviens, soit
dans le sang périphérique du donneur. Par ailleurs, le sang de cordon ombilical, extrait du cordon ombilical
et du placenta après un accouchement, est une autre source de cellules souches progénitrices utilisées en
pratique clinique pour les greffes allogéniques.6 Quand deux autogreffes sont pratiquées de façon planifiée et
séquentielle, le processus est appelé « autogreffe de cellules souches en tandem »6,7
Pendant les trois décennies qui ont suivi la première utilisation réussie d’autogreffe, l’intérêt de ce traitement
dans les pathologies malignes et non malignes a été bien établi (Tableau 1)8. En cas de rechute de pathologies
malignes, les chimiothérapies standards peuvent provoquer des niveaux inacceptables de suppression de la
moelle osseuse (myélosuppression), entraînant une leucopénie, une thrombocytopénie, ainsi qu’une anémie.
Cela augmente le risque d’infections, potentiellement mortelles, et de saignements. Après une chimiothérapie,
le patient reçoit donc une greffe de cellules souches afin de régénérer la moelle osseuse endommagée.
Ainsi, la ré-injection de cellules souches autologues est devenue une stratégie thérapeutique permettant de
raccourcir la période de myélosuppression.9,11 Les données montrent qu‘un traitement à haute dose associé à
des cellules souches de sauvetage a un impact positif sur le taux de réponse de la maladie. Néanmoins, chez
certains patients, cette association ne permet pas d’améliorer la survie globale par rapport aux chimiothérapies
conventionnelles. Ainsi, le rôle définitif de l’autogreffe dans certaines situations, telles que le traitement du
lymphome de Hodgkin réfractaire ou en rechute, ou la leucémie lymphocytaire chronique reste en suspens12–15 et
les indications de l’autogreffe continuent à évoluer.
Chapitre 1 : Synthèse sur l’autogreffe de cellules souches hématopoïétiques 1Tableau 1. Indications de l’autogreffe des cellules souches hématopoïétiques chez l’adulte8
Option, basée sur Nécessité d’études Généralement non
Maladie Traitement standard un rapport bénéfice ou d’investigations
supplémentaires recommandé
/ risque
Leucémie aiguë RC1 (risque standard, intermédiaire RC2 (rechute naissante)
lymphoblastique ou élevé) Maladie en rechute ou réfractaire
Leucémie aiguë myéloïde RC1 (risque intermédiaire) RC1 (risque faible RC3 (rechute naissante)
M3 (RC2 moléculaire) ou élevé) M3 (persistance moléculaire)
RC2 Maladie en rechute ou réfractaire
Leucémie lymphoïde Maladies de faible risque
chronique
Leucémie myéloïde Première (PC), échec à l’imatinib Crise blastique
chronique Phase accélérée ou > première PC
Myélofibrose primaire ou secondaire avec
un score de Lille intermédiaire
ou élevé
Syndrome AREBt AR
myélodysplasique LAMs en RC1 ou RC2 AREB
Stades plus avancés
LNH diffus à grandes Rechute chimiosensible ; RC1 (IPI intermédiaire Maladie réfractaire
cellules ≥ RC2 ou élevé au diagnostic)
Lymphome du manteau RC1 Maladie réfractaire
Rechute chimiosensible ;
≥ RC2
Lymphome RC1 Maladie réfractaire
lymphoblastique Rechute chimiosensible ;
et lymphome de Burkitt ≥ RC2
LNH folliculaire à Rechute chimiosensible ; RC1 (IPI intermédiaire Maladie réfractaire
cellules B ≥ RC2 ou élevé au diagnostic)
LNH à cellules T RC1 Rechute chimiosensible ; ≥ RC2 Maladie réfractaire
Lymphome de Hodgkin Rechute chimiosensible ; Maladie réfractaire RC1
≥ RC2
Lymphome de Hodgkin Rechute chimiosensible ; RC1
nodulaire à prédomi- ≥ RC2
nance lymphocytaire Maladie réfractaire
Myélome multiple
Amylose
Anémie aplasique sévère
Hémoglobinurie
paroxystique nocturne
Cancer du sein* Situation adjuvante à Réaction métastatique
haut risque
Réaction métastatique
Tumeurs à cellules réfractaires de Rechutes sensibles
germinales troisième ligne
Cancer de l’ovaire RC/RP Rechute sensible au platine
Méduloblastome* Post-chirurgie Post-chirurgie
Cancer du poumon à Maladie limitée
petites cellules
Carcinome à cellules Métastatiques, réfractaire aux
rénales cytokines
Sarcome à cellules Réaction métastatique
molles
Cytopénies immunes
Sclérose systémique
Arthrite rhumatoïde
Sclérose multiple
Lupus érythémateux
systémique
Maladie de Crohn
Polyradiculoneuropathie
inflammatoire
démyélinisante chronique
PC, phase chronique ; RC1, 2, 3, première, deuxième ou troisième rémission complète ; RC/RP, réponse complète/réponse partielle ; IPI, Index
pronostique international ; LNH, lymphome non hodgkinien ; AR anémie réfractaire ; AREB, anémie réfractaire avec excès de blastes ; AREBt, anémie
réfractaire avec excès de blastes en transformation ; LAMs, leucémie aiguë myéloïde secondaire ; indique l’utilisation de l’autogreffe de cellules
souches hématopoïétiques quel que soit le grade.
*Chez les patients présentant un cancer du sein métastatique répondeur ou avec médulloblastome, l’autogreffe de cellules souches
hématopoïétiques peut être envisagée si les avantages dépassent les risques, bien que des études supplémentaires soient encore nécessaires.
2 Cellule souche hématopoïétique Mobilisation et cytaphérèse :
Guide pratique à l’usage des infirmiers et autres professionnels paramédicauxUne autogreffe est un processus complexe impliquant une approche et des ressources multidisciplinaires. Sur le
plan historique, ce traitement était proposé uniquement dans les centres hospitaliers universitaires. Néanmoins,
avec les progrès de la médecine et des connaissances sur les procédures d’autogreffe, les patients peuvent
désormais recevoir ce traitement dans des hôpitaux généraux. Le processus de la greffe de cellules souches
peut être résumé en huit étapes distinctes (Figure 1) : (1) administration des traitements de mobilisation, (2)
mobilisation, (3) collecte, (4) préparation du produit pour la conservation, (5) cryoconservation, (6) traitement
myéloablatif, (7) greffe de cellules souches et 8) prise de greffe et récupération.1,2,6,16
Pour de plus amples informations sur chaque étape, veuillez consulter le chapitre 3.
Figure 1. Le processus de greffe de cellules souches1,2,6,16
Injections Mobilisation Collecte
1 2 3
Vaisseau
sanguin
Moelle
osseuse
Injections des traitements de mobilisation Les cellules souches sont stimulées pour qu’elles Collecte des cellules souches mobilisées dans le
migrent de la moelle osseuse vers le système sanguin sang en utilisant une machine de cytaphérèse
Préparation pour la Chimiothérapie
conservation Cryoconservation et/ou irradiation
4 5 6
Les cellules souches prélevées sont stockées dans Congélation des cellules souches pour utilisation Administration du traitement myéloablatif destiné
des poches de perfusion après réalisation du traitement myéloablatif à éradiquer d’éventuelles cellules cancéreuses
résiduelles et à préparer la moelle à accueillir les
nouvelles cellules
Greffe des cellules souches Prise de greffe et récupération
7 8
de neutrophiles (NAN)
Numération absolue
500 20 000
Plaquettes
Suivi après transplantation Suivi après transplantation
Les cellules souches précédemment prélevées sont L’un des objectifs de l’autogreffe de cellules souches est de permettre aux cellules greffées de se transformer en cellules
décongelées puis ré-injectées dans le système sanguin matures et fonctionnelles, telles que les neutrophiles et les plaquettes. Les premiers signes de prise de greffe et de récupération
hématologique se traduisent par l’élévation de la numération absolue des neutrophiles et des plaquettes
Chapitre 1 : Synthèse sur l’autogreffe de cellules souches hématopoïétiques
3Dès que les patients sont identifiés comme candidats à une autogreffe, ils subissent des examens permettant
de s’assurer de leur capacité à tolérer la procédure. Des médicaments sont administrés aux patients pour
stimuler la migration des cellules souches de la moelle osseuse vers le sang périphérique. Ces cellules sont alors
prélevées par cytaphérèse. À l’issue de la cytaphérèse, les cellules sont traitées, puis cryoconservées en vue
d’une utilisation future. Habituellement, la durée de conservation varie de quelques semaines à quelques mois,
bien que certains chercheurs aient rapporté avoir conservé le produit pendant 14 ans sans que celui-ci ne perde
sa viabilité .17-19 Après une cytaphérèse, les patients peuvent recevoir une chimiothérapie additionnelle pour
traiter une maladie sous-jacente ou peuvent directement recevoir traitement myéloablatif pré-greffe (c.-à-d.,
chimiothérapie à haute dose ± radiothérapie) suivi de l’injection des cellules souches précédemment collectées.
Les premiers signes de prise de greffe sont une augmentation de la formule leucocytaire, survenant en général
entre deux à quatre semaines après l’injection de cellules souches autologues.1,2
4 Cellule souche hématopoïétique Mobilisation et cytaphérèse :
Guide pratique à l’usage des infirmiers et autres professionnels paramédicauxChapitre 2 : Mobilisation
L’hématopoïèse désigne la fabrication des différents composants cellulaires du sang. Il s’agit d’un processus
continu qui permet le maintien du fonctionnement normal du système immunitaire et de l’hémostase. Chez
l’adulte, l’hématopoïèse se produit principalement dans la moelle osseuse du pelvis, du sternum, de la colonne
vertébrale et du crâne.20,21 La fabrication de cellules sanguines matures se situe spécifiquement dans le
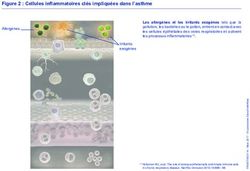
microenvironnement de la moelle osseuse (Figure 2).20-22
Figure 2. Microenvironnement de la moelle osseuse20-22
Mobilisation
Chapitre 2 :
Cellules souches
hématopoïétiques
Vaisseau
sanguin
Cellules stromales
Ostéoclaste
Matrice osseuse
Toutes les cellules sanguines sont dérivées des cellules souches, également appelées cellules souches
pluripotentes. Ces cellules ont une capacité d’auto renouvellement illimitée, ainsi qu’une capacité de se
différencier en tout type de cellule sanguine mature. La cellule souche pluripotente peut se différencier en
un des deux types de cellules souches communes - la cellule souche myéloïde commune et la cellule souche
lymphoïde commune. Ces cellules souches communes peuvent ensuite se différencier en cellules sanguines
via une cascade complexe d’évènements (Figure 3). Le résultat final est la fabrication de cellules myéloïdes
et lymphoïdes. Les cellules myéloïdes, telles que les globules rouges, les plaquettes, les macrophages et les
neutrophiles sont responsables de la régénération des tissus, de l’oxygénation, de la viscosité du sang, de la
coagulation et de la fonction immunitaire telle que l’immunité innée et acquise. Les cellules lymphoïdes,
notamment les cellules T et les cellules B, font partie de la base du système de l’immunité acquise.2,20
Les cytokines jouent un rôle majeur dans l’hématopoïèse. Quand les cellules souches sont exposées
aux cytokines, la cascade de maturation visant à produire les différentes cellules sanguines engagées est
déclenchée. Des exemples de cytokines importantes sont listés dans la Figure 3. Ces cytokines sont endogènes,
bien que pendant le processus de collecte de cellules souches, certaines cytokines exogènes sont administrées
aux patients, afin d’améliorer le rendement des cellules souches dans un court laps de temps.21-25 Ces cytokines
exogènes comprennent le filgrastim (facteur de croissance granulocytaire [G-CSF] glycosylé) et le lénograstim
(G-CSF non glycosylé).
Chapitre 2 : Mobilisation 5Figure 3. Cascade de maturation de la cellule souche2,20
Cellule souche hématopoïétique
Différenciation Différenciation
Cellules précurseurs lymphoïdes dédiées Cellules précurseurs myéloïdes dédiées
IL-2 SCF GM-CSF
IL-7 Cytokines Epo
Tpo IL-3
IL-12 GM-CSF
M-CSF IL-3 G-CSF
Supplémentaire
Monocyte/ Globule Plaquettes Éosinophile
Cellule B Cellule T Granulocyte
macrophage rouge
Cellules différenciées
Epo, érythropoïétine ; G-CSF, facteur de croissance granulocytaire, GM-CSF, facteur de croissance granulocyte-macrophage ;
IL, interleukine ; M-CSF, facteur de croissance des macrophages ; FCS, facteur de cellule souche ; Tpo, thrombopoïétine.
Les chimiokines font partie d’un sous-groupe de cytokines associées à un seul récepteur et contribuant à
la migration de la cellule. Les cellules stromales sont des couches de cellules responsables du maintien du
microenvironnement de la moelle osseuse. Ces cellules sécrètent de la chimiokine SDF-1a. Cette chimiokine
est une molécule de signalisation importante responsable de la prolifération, de l’écotropisme et de la prise
de greffe des cellules souches. A un moment spécifique de leur développement, les cellules souches expriment
le récepteur de chimiokine CXCR4. Le CXCR4 est responsable de l’ancrage des cellules souches dans le
microenvironnement de la moelle osseuse. Quand le CXCR4 et le SDF-1a se lient, des interactions entre les
intégrines et les molécules d’adhésion cellulaire se produisent également. L’ancrage des cellules souches au
sein du microenvironnement de la moelle osseuse survient grâce à la production continue de SDF-1a par les
cellules stromales. C’est la perte d’ancrage aux cellules stromales, ainsi que la perte de l’activité de SDF-1a qui
favorisent la libération des cellules souches dans la circulation périphérique. Un blocage de ce récepteur avec
un antagoniste de la chimiokine (tel que le plérixafor) provoque une augmentation de la quantité de cellules
souches hématopoïétiques (CSH) et permet la collecte de cellules souches chez les patients présentant un
myélome et un lymphome multiple.26-31
6 Cellule souche hématopoïétique Mobilisation et cytaphérèse :
Guide pratique à l’usage des infirmiers et autres professionnels paramédicauxLes cellules souches pluripotentes expriment le marqueur antigénique CD34. Ce marqueur est l’indicateur le plus
souvent utilisé en pratique clinique pour déterminer l’ampleur et l’efficacité des collectes de cellules souches
périphériques.25 Bien qu’ils ne représentent pas une mesure exacte de la qualité et de la quantité des cellules
prélevées, les échantillons sanguins issus des collectes sont analysés afin de déterminer le nombre de cellules
CD34+ présentes. Dès que l’objectif spécifique du nombre de cellules est atteint, les collectes de cellules sont
arrêtées et conservées pour une utilisation future. Les objectifs cibles peuvent varier en fonction des centres de
traitement et l’objectif spécifique du patient est lié à la maladie sous-jacente, la source des cellules souches et le
type de greffe à pratiquer. En général, un objectif de 2 × 106 CD34+ cellules/kg de poids corporel est considéré
comme minimum pour une autogreffe avec un objectif optimal de ≥ 5 × 106 CD34+ cellules/kg pour une seule
greffe et de ≥ 6 × 106 CD34+ cellules/kg pour une greffe en tandem.23,25,32-36
Historiquement, les prélèvements des cellules Figure 4. Prélèvement de la moelle
souches autologues impliquaient le prélèvement de la osseuse
moelle osseuse de la région postérieure de la crête
iliaque du patient (Figure 4) sous anesthésie générale
au bloc opératoire. Néanmoins, avec les progrès de
la technologie médicale, la plupart des prélèvements
sont maintenant effectués par cytaphérèse (Figure 5).
Le prélèvement des cellules souches du sang
périphérique est considéré comme la méthode de
choix pour la mobilisation avant une ACSH, permettant
le confort du patient, une diminution de la morbidité
et une prise de greffe rapide des leucocytes et des
plaquettes. D’autres éléments de comparaison entre
le prélèvement de la moelle osseuse et du sang
périphérique pour une transplantation autologue sont
résumées dans le Tableau 2.1,2,37-40
Tableau 2. Avantages et inconvénients des
méthodes de collecte des cellules souches
hématopoïétiques1,2,37-40
Méthode
Avantages Inconvénients
de collecte
Moelle • Collecte unique • Pratiqué dans un établissement ayant une structure
osseuse de soins intensifs en raison de l’anesthésie générale
• Mise en place spéciale de cathéter non
requise • Prise de greffe de neutrophiles et de plaquettes plus
• Utilisation des cytokines non requise lente
• Taux de morbidité et de mortalité plus élevés
• Contamination du produit par les cellules tumorales
potentiellement plus élevée
Sang • Anesthésie générale non requise et • La collecte peut durer plusieurs jours
périphérique possibilité d’être effectuée en consultation • Nécessite parfois la mise en place de cathéter à gros
externe calibre et à double lumière pour la collecte
• Prise de greffe de neutrophiles et de • Les hémorragies, les embolies et les infections sont
plaquettes plus rapide des complications possibles liées à l’insertion du
• Associé à des taux de morbidité et de cathéter veineux central
mortalité inférieurs
• Contamination du produit par les cellules
tumorales potentiellement moins élevée
Chapitre 2 : Mobilisation 7Figure 5. Collecte par cytaphérèse
Les concentrations des CSH sont de
10 à 100 fois supérieures dans la
moelle osseuse que dans la circulation
périphérique.1 Par conséquent, des
méthodes permettant d’augmenter les
concentrations des CSH circulantes
sont nécessaires afin d’assurer des
collectes satisfaisantes. Les traitements
pour mobiliser les CSH incluent
l’administration de cytokines avec ou
sans chimiothérapie préalable aux
périodes de collecte.
L’utilisation de filgrastim et de lénograstim seuls comme mobilisateurs est bien établie ; ces deux agents ayant
démontré de façon reproductible des concentrations élevées de CSH circulantes.41,42 On pense que le G-CSF
stimule la mobilisation des CSH en diminuant l’expression génétique de SDF-1a et les niveaux protéiniques tout
en augmentant les protéases qui peuvent cliver les interactions entre les CSH et l’environnement de la moelle
osseuse.43-46 Le mécanisme d’action du G-CSF est illustré dans la Figure 6.43-46 La dose recommandée de filgrastim
et de lénograstim est de 10 mcg/kg/j par injection sous-cutanée pendant plusieurs jours.47,48 Cependant, ces
facteurs de croissance sont typiquement administrés à une dose quotidienne totale de 3-24 mcg/kg/j.25 Les
données indiquent que des doses divisées de G-CSF (par ex., lénograstim 5 mcg/kg deux fois par jour) sont plus
efficaces que l’administration d’une dose unique (par ex., lénograstim 10 mcg/kg quotidiennement) en raison
d’un rendement supérieur de cellules CD34+ avec moins de cytaphérèse.49-51 Toutefois, la pratique clinique
courante ne favorise aucune des deux approches.
Figure 6. Mécanisme d’action du G-CSF43-46
Vaisseau sanguin
Moelle osseuse
G-CSF
Neutrophile
Cellules CD34+
Prolifération Libération de protéases
CXCR4
Molécule d'adhésion
SDF-1α
Cellule stromale
Ostéoblaste
CXCR4, récepteur 4 de chimiokine ; G-CSF, facteur de croissance granulocytaire ; SDF-1α, facteur-1 alpha dérivé de la cellule stromale.
8 Cellule souche hématopoïétique Mobilisation et cytaphérèse :
Guide pratique à l’usage des infirmiers et autres professionnels paramédicauxComme il est fréquent d’observer une augmentation des CSH après un traitement par chimiothérapie
myélosuppressive, une méthode alternative de mobilisation des CSH consiste à administrer une chimiothérapie
en association aux cytokines.22,24,25 Ce procédé est souvent appelé « chimiomobilisation ». La chimiothérapie
et les cytokines agissent en synergie pour mobiliser les CSH, bien que le mécanisme exact de la mobilisation
par chimiothérapie ne soit pas totalement connu. Les mécanismes possibles de la mobilisation après une
chimiothérapie incluent les effets de la chimiothérapie sur l’expression des molécules d’adhésion cellulaire dans
la moelle osseuse et les dommages induits par la chimiothérapie sur les cellules stromales de la moelle osseuse.
Ces deux mécanismes produisent des concentrations élevées de CSH circulantes dues à la perturbation du
microenvironnement de la moelle osseuse.28 La cinétique de la production des cellules CD34+ et des leucocytes
après une chimiothérapie et l’administration de facteurs de croissance sont illustrées dans la Figure 7.
Figure 7. Cinétique généralisée du leucocyte et de la cellule Les agents chimiothérapeutiques
CD34+ Mobilisation dans le sang périphérique après une les plus couramment utilisés
en chimiomobilisation sont le
chimiothérapie et l’administration de cytokines
cyclophosphamide et l’étoposide
à haute dose.22,25,38 Le filgrastim
Leucocytes
Cellules CD34+ (5 mcg/kg/j) peut être utilisée la
Aphérèse cytokine dans la chimiomobilisation.47
Niveau cellulaire
Comme aucune chimiothérapie
de mobilisation n’a démontré de
supériorité par rapport aux autres,
certains cliniciens choisissent
d’utiliser la chimiothérapie dédiée
1 5 10 à la maladie pour la mobilisation.
Nombre de jours après l'administration de la chimiothérapie Des exemples d’associations
ainsi utilisées sont le protocole
Chimiothérapie G-CSF cyclophosphamide, doxorubicine,
vincristine, prédnisone (CHOP)
G-CSF, facteur de croissance granulocytaire.
ou le protocole infosfamide,
carboplatine, étoposide (ICE).25
De plus, l’utilisation de rituximab (un anti-corps monoclonal dirigé vers les cellules exprimant le CD20)
avant la mobilisation n’a démontré aucun rendement inférieur de cellules CD34+. En fait, il peut aider à
réduire la contamination tumorale du greffon infecté.52,53 Les évènements indésirables associés aux agents
chimiothérapeutiques couramment utilisés lors de la mobilisation sont listés dans le Tableau.54,55
Tableau 3. Complications* associées aux agents chimiothérapeutiques couramment utilisés
pour la mobilisation (par exemple le cyclophosphamide ou l’étoposide)54,55
Effets secondaires à court terme Effets secondaires à long terme
• Malaise général (faiblesse) • Miction réduite (peut indiquer une
• Infertilité lésion rénale)
• Symptômes GI (diarrhées, nausées, vomissements, perte d’appétit, gêne • Difficulté respiratoire ou œdème
ou douleur d’estomac) (peuvent indiquer une insuffisance
• Effets cutanés et de la muqueuse (érythème, modification de la texture cardiaque congestive)
des ongles, alopécie, inflammation de la muqueuse) • Malignités secondaires (peuvent
• Myélosuppression (thrombocytopénie, leucopénie) se présenter sous forme de
• Effets secondaires liés à l’injection (tels que hypertension artérielle, nævus inhabituels, de plaies
bouffées vasomotrices, douleur thoracique, fièvre, diaphorèse, cyanose, cutanées non cicatrisantes ou de
urticaire, angio-œdème et bronchospasme) plastrons inhabituels)
• Réaction allergique
• Signes d’infection, par exemple frissons ou fièvre
• Sang dans l’urine (peut indiquer une lésion de la vessie)
• Sang dans les selles
GI, gastro-intestinal.
* Merci de consulter les monographies des produits concernés pour une liste complète des réactions indésirables.
Chapitre 2 : Mobilisation 9Le plérixafor est un nouvel agent récemment Figure 8. Mécanisme d’action du plérixafor57-61
autorisé par l’Union européenne en association
avec le G-CSF chez les patients présentant ou
un lymphome ou un myélome multiple dont Vaisseau sanguin
les cellules se mobilisent mal, dans le but de
mobiliser les cellules de la moelle osseuse
dans le sang périphérique pour une collecte et
Moelle osseuse
une autogreffe.56 Le plérixafor est une petite
molécule antagoniste du CXCR4 qui inhibe
réversiblement l’interaction entreNeutrophil
le CXCR4 Plérixafor
Plerixafor
et le SDF-1a (voir le mécanisme d’action du
plérixafor à la Figure 8).57-61 Il a été démontré
que l’utilisation du plérixafor en association
Cellules CD34+
avec le G-CSF améliorait la collecte de cellules CXCR4
CD34+ chez les patients présentant un
lymphome ou un myélome multiple par rapport
à l’utilisation du G-CSF seul.30,62,63 Les effets
secondaires indésirables associés à l’utilisation SDF-1α
du filgrastim, du lénograstim, et du plérixafor
sont listés dans le Tableau 4.47,48,56,64
Un inconvénient de la collecte des CSH est
le mauvais rendement des cellules souches.
Le facteur de risque le plus important d’une
mobilisation inadéquate est le nombre de Cellules stromales
séances de chimiothérapie myélosuppressive
Osteoblast
CXCR4, récepteur 4 de chimiokine; SDF-1α, facteur 1-alpha dérivé de la
administrées au patient avant la collecte. Les
cellules stromale
agents toxiques pour les cellules souches,
tels que le cyclophosphamide (doses > 7,5 g/m2), le melphalan, la carmustine, le procarbazine, la fludarabine,
la moutarde azotée et le chlorambucil sont particulièrement nuisibles au rendement des collectes de cellules
souches. D’autres facteurs de risque associés à une collecte moins importante de cellules CD34+ sont listés
dans le Tableau 5.25,65-73
Tableau 4. Réactions indésirables* très fréquentes (> 10 %) associées aux agents utilisés dans
la mobilisation des cellules souches47,48,56,64
Agent Événements indésirables
Filgrastim • Douleur musculosquelettique
Lénograstim • Douleur osseuse et dorsale
• Leucocytose et thrombocytopénie
• Hausses passagères des tests de la fonction hépatique
• LDH élevée
• Céphalée et asthénie
Plérixafor • Diarrhée et nausée
• Réactions sur les sites d’injection et de perfusion
LDH, lactodéshydrogénase.
* Merci de consulter les résumés des monographies des produits pour obtenir une liste complète des réactions indésirables.
10 Cellule souche hématopoïétique Mobilisation et cytaphérèse :
Guide pratique à l’usage des infirmiers et autres professionnels paramédicauxTableau 5. Facteurs de risque et caractéristiques associés à une faible mobilisation des
cellules souches25,65-73
• Type et nombre de séances de chimiothérapie administrées au patient avant la mobilisation
• Âge avancé (> 60 ans)
• Cycles multiples de chimiothérapie préalables au traitement de la maladie sous-jacente
• Radiothérapie
• Intervalle de temps court entre la chimiothérapie et la mobilisation
• Maladie extensive
• Maladie réfractaire
• Infiltration tumorale de la moelle osseuse
• Utilisation préalable de lénalidomide
• Indication de mauvais fonctionnement de la moelle osseuse (par ex. faible taux de plaquettes et de cellules CD34+
à la numération) au moment de la mobilisation
Peu d’options sont disponibles pour les patients présentant une faible mobilisation et la prise en charge
standard de ces patients continue d’évoluer et reste mal définie. Les stratégies couramment utilisées pour
la remobilisation comprennent l’élévation des doses des agents de chimiothérapie et/ou des cytokines,
l’association de plusieurs cytokines, ainsi que l’allongement du temps entre le traitement chimiothérapique de
la maladie et la cytaphérèse. Une stratégie alternative consiste à prélever des cellules de la moelle osseuse.
Cependant, elle perd de son importance vis-à-vis des méthodes mentionnées précédemment en raison d’une
prise de greffe plus lente, besoin supérieur en ressources (hospitalisation prolongée et prise en charge
thérapeutique plus conséquente) et un risque plus élevé de mortalité.25,35,65,66,74-76 Les nouveaux agents récemment
autorisés (tel que le plérixafor) semblent prometteurs dans le cadre des techniques de mobilisation établies
pour augmenter le rendement des cellules souches pendant la collecte. Une comparaison entre les méthodes de
mobilisation est listée dans le Tableau 6.22,24,25,28,37-39
Tableau 6. Comparaison des méthodes de mobilisation22,24,25,28,37-39,77-81
Régime de mobilisation Caractéristiques
Filgrastim ou lénograstim • Administration en consultation externe
• Peut être auto-administré
• Efficacité élevée chez la plupart des patients
• Mobilisation prévisible, permettant une planification facile de la cytaphérèse
• Durée moins importante entre l’administration et la collecte par rapport à
l’utilisation de facteur de croissance + chimiothérapie
• Douleur osseuse
• Faible rendement de cellules souches par rapport à l’utilisation de facteur de
croissance + chimiothérapie
Filgrastim ou lénograstim + • Rendement plus élevé de cellules souches par rapport à l’utilisation du
chimiothérapie facteur de croissance seul
• Collecte de cellules souches inférieure
• Potentiel pour des activités anti-cancéreuses
• Peut détériorer une future mobilisation de cellules souches
• Peut nécessiter une hospitalisation
• Associé à un nombre croissant d’effets indésirables
• Résultats contradictoires
• Durée plus importante entre l’administration et la collecte par rapport à
l’utilisation de facteur de croissance
• Faible prévisibilité de la durée nécessaire pour atteindre le niveau maximum
de cellules CD34+ du sang périphérique
Filgrastim ou lénograstim + • Faible toxicité
plérixafor • Administration en consultation externe
• Faible taux d’échec
• Probabilité élevée de prélèvement du nombre optimal de cellules CD34+
• Efficace chez les faibles mobilisateurs
• Mobilisation prévisible, permettant une planification facile de la cytaphérèse
• Durée plus courte entre l’administration et la collecte par rapport à
l’utilisation de facteur de croissance + chimiothérapie
• Effets gastro-intestinaux indésirables
Chapitre 2 : Mobilisation 11Chapitre 3 : Collecte de cellules souches (cytaphérèse),
conservation et ré-injection
Avant l’initiation du processus de collecte de cellules souches, les patients doivent être examinés attentivement
afin de déterminer les candidats aptes à recevoir une greffe et capables de tolérer l’ensemble des procédures.
Certaines des évaluations médicales, infirmières et psychologiques peuvent s’effectuer avant qu’il ne soit dirigé
vers un service de greffe. L’hématologue/oncologue traitant du patient sert souvent de premier contact pendant
le processus de greffe. Toutes les analyses, évaluations et préparations du patient, nécessaires au cours de la
greffe, impliquent de nombreux professionnels des soins de santé travaillant ensemble pour coordoner cette
procédure médicale complexe.
La pré-évaluation médicale constitue la première étape que doit effectuer le patient avant une CSH. Cela signifie
que l’oncologue traitant du patient doit le recommander à un centre ou à un service de greffe. Le médecin
référant doit fournir à l’équipe de greffe toutes les informations spécifiques concernant les soins prodigués
jusqu’à présent, ses antécédents médicaux, le stade de son cancer, un résumé des traitements et des réponses
aux anti-cancéreux et les complications survenues pendant les traitements. Tous les clichés radiographiques et
résultats des analyses de laboratoire disponibles doivent accompagner ces informations.
Après avoir pris connaissance des informations concernant le patient, l’équipe de greffe met en œuvre sa
propre batterie de tests et d’évaluations afin de décider si le patient est éligible à une collecte et à une
greffe de cellules souches. Cela implique une réévaluation du stade actuel de la maladie, une évaluation
du fonctionnement de divers organes (par ex. reins, foie et poumons), une documentation sur l’absence de
Collecte de cellules souches,
conservation et réinjection
certaines conditions de comorbidités et de maladies infectieuses (par ex. insuffisance cardiaque congestive,
VIH) et une évaluation de l’état général psychosocial du patient. Dès lors, une information complète débutera à
Chapitre 3 :
l’intention du patient, de sa famille et/ou de ses professionnels de santé. Souvent un membre de la profession
infirmière (infirmier clinique, infirmier éducateur ou infirmier coordinateur) coordonnera le processus
d’éducation du patient et de ceux impliqués dans son traitement (voir Chapitre 4).
Dès que le patient est déclaré éligible à une greffe, sa préparation au processus de collecte peut commencer.
La méthode privilégiée pour l’accès veineux est la mise en place d’un cathéter périphérique au moment de la
phase de cytaphérèse (par ex. insertion dans la veine cubitale antérieure). Pour les patients chez lesquels un
accès périphérique n’est pas faisable, une sélection appropriée de cathéter et une mise en place d’un accès
veineux central (par ex. veine jugulaire interne) sont planifiées avant la première collecte de cellules souches.
Les cathéters utilisés pour une cytaphérèse doivent être capables de supporter de grandes fluctuations du
volume sanguin circulant. De ce fait, ces cathéters sont souvent des dispositifs à gros calibre et à double
lumière qui peuvent être utilisés temporairement pour la collecte ou placés de façon permanente durant tout
le processus de greffe. Tout comme avec la plupart des cathéters placés aux membres supérieurs, les patients
doivent être suivis pour des signes et symptômes d’hypertension artérielle, d’essoufflements et de diminution
du bruit respiratoire, qui sont des indications de perforation de la paroi veineuse, d’hémothorax et/ou de
pneumothorax tous rares, mais constituant des complications sérieuses pouvant survenir. Dans certains cas,
les cathéters à cytaphérèse peuvent être placés centralement dans une veine fémorale si le patient présente
un risque élevé de développer des complications avec le cathéter placé aux membres supérieurs ou sur la paroi
thoracique. Pour les cathéters placés centralement, une évaluation radiographique est réalisée afin de vérifier
son positionnement avant son utilisation. De plus, les instructions sur l’entretien du cathéter, afin de prévenir
toute infection et de maintenir son intégrité, doivent être revues avec le patient et /ou les professionnels de
santé.1,2,16,82,83
La préparation à la collecte de cellules souches dans un centre ou un service pratiquant la cytaphérèse est
réalisée après l’évaluation pré-greffe et la mise en place du cathéter. Les patients sont informés et conseillés
sur le traitement qu’ils reçoivent pendant la mobilisation, le calendrier d’administration et les effets indésirables
prévus. Comme indiqué dans le Chapitre 2, les agents utilisés pendant cette phase de l’autogreffe comprennent
généralement une cytokine (tel que le filgrastim) administrée seule avec ou sans chimiothérapie spécifique, ou
suivant, chimiothérapie dédiée à la maladie ou enfin plus récemment, du filgrastim ou du lénograstim associé
Chapitre 3 : Collecte de cellules souches (cytaphérèse), conservation et ré-injection 13au plérixafor. Selon le choix du schéma de mobilisation, les patients peuvent avoir leur première séance de
cytaphérèse après quatre à cinq jours ou, dans certains cas, après deux à trois semaines.1,16,83 La durée de
la mobilisation est déterminée par l’évaluation de la numération leucocytaire du patient. Des numérations
leucocytaires en série permettent au clinicien de déterminer le moment approprié pour le début des collectes.
Certains centres de collecte peuvent utiliser le taux de cellules CD34+ périphériques comme marqueur de
l’état de mobilisation. Le seuil d’initiation de la cytaphérèse peut varier d’un centre à l’autre, se situent entre 5
et 20 cellules CD34+/microlitre. Bien qu’elles soient utiles dans l’estimation de l’efficacité de la mobilisation,
les numérations des cellules CD34+ du sang périphérique peuvent varier d’un centre à l’autre ou au sein d’un
même centre.35,84,85
Figure 9. Exemple d’une machine de cytaphérèse Lorsque la mobilisation atteint son niveau optimal,
le patient peut être planifié pour des séances de
collecte dans le centre de cytaphérèse. Un technicien
en cytaphérèse spécialisé dans la collecte de cellules
souches est responsable du matériel utilisé dans
le processus de collecte (Figure 9). Les infirmiers
cliniques au sein du service de cytaphérèse sont
tenus d’informer le patient sur le processus
de collecte et de le surveiller afin de détecter
d’éventuels signes de réactions indésirables. Les
patients sont reliés à la machine de cytaphérèse par
leur cathéter. Une ligne est utilisée pour transférer
le sang du patient à la machine. Là, le sang est
centrifugé dans une chambre de centrifugation
située dans le séparateur de cellules de la machine.
Les cellules souches désirées sont collectées
pendant toute la procédure, soit par cycles, soit
continuellement et les composants sanguins restants
sont réinjectés au patient par la seconde ligne de son
cathéter. Cette seconde ligne peut aussi être utilisée
pour l’administration de solutions intraveineuses,
de suppléments électrolytiques et de médicaments.
Chaque séance de cytaphérèse dure environ deux à cinq heures, durant lesquelles plus de trente litres de sang ou
six fois le volume sanguin moyen traités. La collecte peut s’effectuer quotidiennement jusqu’à ce que les objectifs
cibles de cellules CD34+ soient atteints. Le processus de cytaphérèse peut durer jusqu’à quatre jours en fonction des
caractéristiques du patient et du régime de mobilisation utilisé.2,16,17,82,86-88
Les protocoles de cytaphérèse sont relativement sûrs. Bien que le taux de mortalité soit très faible et estimé à
trois décès pour 10 000,89 la cytaphérèse est associée à quelques morbidités. Le citrate est un anti-coagulant uti-
lisé pendant le processus de cytaphérèse afin d’empêcher la coagulation du sang. Ainsi, l’un des effets indésirables
les plus communs survenant pendant ce processus, est la toxicité liée au citrate qui se manifeste par une hypocal-
cémie, à la liaison du calcium sérique ionisé. Les signes et symptômes de la toxicité au citrate, ainsi que sa prise en
charge sont détaillés dans le Tableau 7. Un suivi de la calcémie avant et pendant tout le processus de cytaphérèse
peut réduire la probabilité d’une hypocalcémie.16,82,90 D’autres effets indésirables de la toxicité au citrate incluent
une hypomagnésémie, une hypokaliémie et une alcalose métabolique. Le magnésium, tout comme le calcium, est
un ion bivalent qui est lié par le citrate. Les diminutions des niveaux de magnésium sérique sont souvent plus pro-
noncées et prennent plus de temps à se normaliser que les anomalies concernant le taux de calcium. Les signes
et symptômes de l’hypomagnésémie, de l’hypokaliémie et de l’alcalose métabolique ainsi que leur prise en charge
sont détaillés dans le Tableau 7.16,82,90
14 Cellule souche hématopoïétique Mobilisation et cytaphérèse :
Guide pratique à l’usage des infirmiers et autres professionnels paramédicauxTableau 7. Les complications courantes liées à la cytaphérèse16,82,90
Effet indésirable Cause Signes et symptômes Action corrective
Toxicité au Anticoagulant (citrate) Hypocalcémie Diminuer le taux d’aphérèse ;
citrate administré pendant la Fréquents : étourdissements, picotements augmenter le rapport sang/
cytaphérèse de la bouche, des mains et des pieds citrate ; traitement de
supplémentation en calcium
Rares : frissons, tremblements, convulsions
et crampes musculaires, crampes
abdominales, tétanie, ictus, arythmie
cardiaque
Hypomagnésémie Diminuer le taux d’aphérèse ;
Fréquents : spasmes musculaires ou augmenter le rapport sang/
faiblesse citrate ; traitement de
supplémentation en magnésium
Rares : diminution de la tonicité vasculaire
Hypokaliémie Diminuer le taux d’aphérèse ;
Fréquents : faiblesse augmenter le rapport sang/
citrate ; traitement de
Rares : hypotonie et arythmie cardiaque supplémentation en potassium
Alcalose métabolique Diminuer le taux d’aphérèse ;
Fréquents : aggravation de l’hypocalcémie augmenter le rapport sang/
citrate
Rares : diminution de la fréquence
respiratoire
Thrombocytopénie Des plaquettes Faible numération plaquettaire, ecchymoses, Préparer la machine à aphérèse
adhèrent à la surface saignements avec des produits sanguins au
interne de la machine à lieu de soluté physiologique ;
cytaphérèse transfusion de plaquettes
Hypovolémie Patient intolérant à Étourdissements, fatigue, sensations Diminuer le taux de la séance
d’importants transferts ébrieuses, tachycardie, hypotension, diapho- d’aphérèse ou l’arrêter
de sang extracorpo- rèse, arythmie cardiaque temporairement ; bolus de
rels et de volumes de liquides intraveineux
plasma
Défaillance du Formation de caillots Incapacité à évacuer le cathéter, accumu- Diminuer le taux de la séance
cathéter de sang ou cathéter lation sous-cutanée de liquide autour de d’aphérèse ou l’arrêter
mal placé pour per- la zone du cathéter ; douleurs et érythème temporairement ; bolus de
mettre un flux sanguin dans la zone du cathéter ; tuméfaction du liquides intraveineux
approprié bras, diminution du flux sanguin
Infection Des agents pathogènes Fièvre, frissons, fatigue, peau rougeâtre et Administrer des antibiotiques ;
microbiens pénètrent érythémateuse autour du cathéter, hypoten- éventuellement enlever le
le sang à travers le sion, hémocultures positives cathéter
cathéter ou le site du
cathéter
Certains patients peuvent subir une hypovolémie due aux importantes fluctuations dans le volume de sang
pendant la cytaphérèse. Les signes et symptômes d’une hypovolémie, ainsi que sa prise en charge sont détaillés
dans le Tableau 7.16,82,90 Avant le début de la cytaphérèse, le pouls et la pression artérielle sont mesurés puis
continuellement évalués à intervalles réguliers. Il est également recommandé que le taux d’hémoglobine
et l’hématocrite soient suivis. Les patients qui risquent de développer une hypovolémie sont les personnes
présentant une anémie ou des antécédents cardiovasculaires et les enfants et adultes de petite taille. Les
mesures préventives tentent de minimiser la variation du volume extracorporel préparant la machine de
cytaphérèse avec des globules rouges et du plasma frais congelé plutôt qu’avec un soluté physiologique normal.
Une hypovolémie peut également être prise en charge en administrant des bolus intraveineux de solutés et
en diminuant le débit du flux de la machine de cytaphérèse. Un autre problème potentiel provoqué par une
hypovolémie est le développement d’une arythmie cardiaque, potentiellement mortelle. En cas de survenue, la
cytaphérèse doit être interrompue et les symptômes doivent avoir disparu avant de poursuivre les collectes.16,82,90
La thrombocytopénie, les infections et la défaillance du cathéter sont autant de complications qui peuvent
survenir pendant la collecte des cellules souches. Lorsque le sang du patient est présent dans le séparateur
de cellules de la machine, les plaquettes peuvent adhérer au dispositif de centrifugation. Des diminutions
dans la concentration de plaquettes peuvent être importantes et il est essentiel d’effectuer des numérations
Chapitre 3 : Collecte de cellules souches (cytaphérèse), conservation et ré-injection 15Vous pouvez aussi lire